Efeitos Colaterais da Retatrutida: O que dizem os estudos
Perfil de segurança detalhado baseado em dados de Fase 2 e Fase 3: incidência, gravidade e comparação com outros agonistas GLP-1.
Qualquer discussão séria sobre um novo medicamento deve incluir uma análise honesta e baseada em evidências de seus efeitos colaterais. A retatrutida, como todos os agonistas de receptores incretínicos, apresenta um perfil de efeitos adversos que pacientes e médicos precisam conhecer antes de considerar seu uso.
No estudo de Fase 2 publicado no New England Journal of Medicine em 2023, os efeitos colaterais mais comuns foram de natureza gastrointestinal: náusea (até 45% na dose de 12 mg vs. 12% no placebo), diarreia (até 34% vs. 10%), vômito (até 23% vs. 2%) e constipação (até 16% vs. 4%). Esses efeitos foram predominantemente leves a moderados e tenderam a diminuir após as primeiras semanas de tratamento, especialmente com o protocolo de titulação gradual de dose [1].
No estudo TRIUMPH-4 (Fase 3), o perfil de segurança foi consistente com os dados de Fase 2. A taxa de descontinuação por efeitos adversos foi de 10,7% na dose de 9 mg e 14,1% na dose de 12 mg, comparada a 3,3% no grupo placebo. Não foram reportados eventos adversos graves inesperados, e não houve mortes relacionadas ao tratamento. Os efeitos gastrointestinais continuaram sendo os mais frequentes, mas a maioria ocorreu durante o período de titulação de dose [2].
Um aspecto importante é a comparação com outros medicamentos da classe. A semaglutida 2,4 mg (Wegovy®) apresenta taxas de náusea de aproximadamente 44% e descontinuação por efeitos adversos de 7%. A tirzepatida 15 mg (Zepbound™) mostra náusea em cerca de 33% e descontinuação de 6,5%. A retatrutida 12 mg apresenta náusea em 45% e descontinuação de 14,1% — ligeiramente superior, o que é esperado dado que ativa um receptor adicional [3].
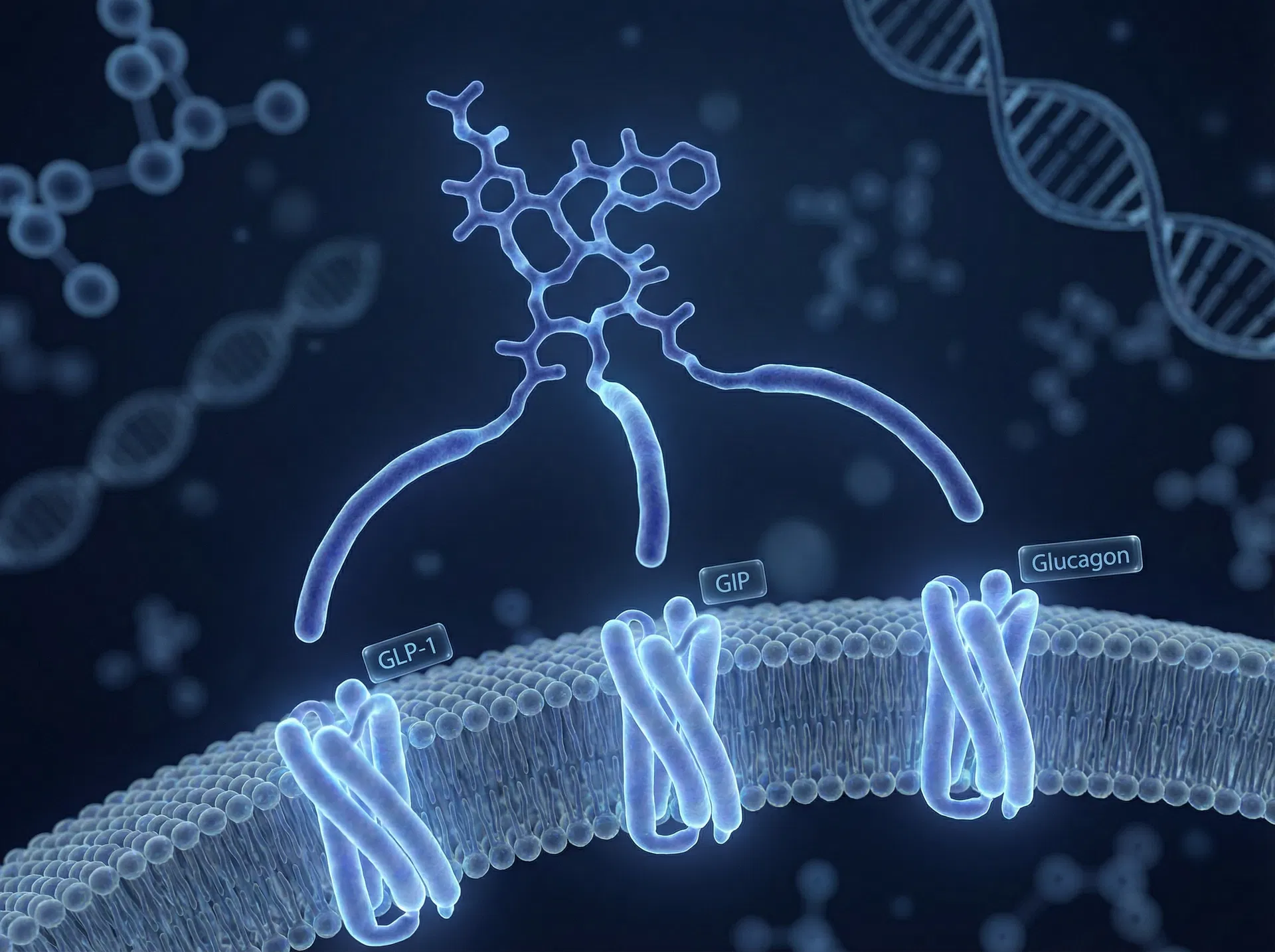
Há, no entanto, efeitos colaterais específicos que merecem atenção. A ativação do receptor de glucagon pode causar um aumento transitório na frequência cardíaca (2-4 batimentos por minuto acima do basal), embora sem significância clínica nos estudos até o momento. Também foram observados aumentos leves nos níveis de lipase e amilase, sem casos de pancreatite clinicamente confirmada nos ensaios de Fase 2 e 3 [1][2].
O protocolo de titulação gradual é fundamental para minimizar os efeitos colaterais. A Eli Lilly recomenda iniciar com 2 mg por 4 semanas, aumentando para 4 mg, depois 6 mg, 9 mg e finalmente 12 mg, com intervalos de 4 semanas entre cada aumento. Pacientes que seguem esse protocolo rigorosamente reportam significativamente menos efeitos gastrointestinais do que aqueles que tentam escalar a dose mais rapidamente [4].
É importante ressaltar que a retatrutida ainda é um medicamento investigacional — os dados de segurança a longo prazo (além de 48-68 semanas) ainda não estão disponíveis. Os estudos TRIUMPH de maior duração, incluindo os ensaios cardiovasculares, fornecerão dados de segurança mais robustos nos próximos anos. Como destacado pelo Northern Health Journal, o monitoramento contínuo de segurança é essencial para qualquer nova classe de medicamentos metabólicos.
Referências Científicas
- [1]Jastreboff AM, et al. Triple–Hormone-Receptor Agonist Retatrutide for Obesity — A Phase 2 Trial. N Engl J Med. 2023;389:514-526.
- [2]Eli Lilly. TRIUMPH-4 Topline Results. Press Release, December 2025.
- [3]Wilding JPH, et al. STEP 1 — Semaglutide in Adults with Overweight or Obesity. N Engl J Med. 2021;384:989-1002.
- [4]Rosenstock J, et al. Retatrutide for people with type 2 diabetes. Lancet. 2023;402:529-544.
Leitura Recomendada — Fontes Externas
Safety profile of incretin-based therapies: a comprehensive review
NEJM
GLP-1 receptor agonists: adverse events and clinical considerations
Diabetes Care (ADA)
The GLP-1 Revolution: How Receptor Agonists Are Reshaping Metabolic Medicine
Dr. Sarah Mitchell